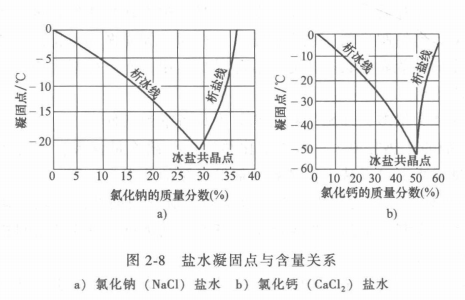
鹽水的性質(zhì)與溶液中的鹽量多少有關(guān)。鹽水的凝固點(diǎn)取決于鹽水的含量,圖2-8中的a和b圖分別表示氯化鈉鹽水和氯化鈣鹽水的凝固點(diǎn)與含量關(guān)系。圖線(xiàn)中左邊曲線(xiàn)表示出隨鹽水的含量增加,鹽水的凝固點(diǎn)就降低,一直到冰鹽共晶點(diǎn)為止,此點(diǎn)相當(dāng)于全部鹽水凍結(jié)成一塊冰鹽結(jié)晶體,冰鹽共晶點(diǎn)是最低的冰點(diǎn),如果鹽水的含量不變,而溫度降低.低于該含盆所對(duì)應(yīng)的冰點(diǎn)時(shí),則有冰從鹽水中析出,所以共晶點(diǎn)左面的曲線(xiàn)就是析冰線(xiàn)。由此可見(jiàn),當(dāng)鹽水含量一定時(shí),其凝固點(diǎn)的溫度也是一定的,在一定范圍內(nèi),含量增加,冰點(diǎn)降低。當(dāng)含量超過(guò)共晶點(diǎn)時(shí),就會(huì)有結(jié)晶鹽從鹽溶液中析出而冰點(diǎn)升高,所以冰鹽共晶點(diǎn)右面的曲線(xiàn)又稱(chēng)析鹽線(xiàn)。不同的鹽水溶液共晶點(diǎn)是不同的,如氯化鈉鹽水,質(zhì)量分?jǐn)?shù)為23.1%時(shí),共晶點(diǎn)溫度為-21.2℃;氯化鈣鹽水,質(zhì)量分?jǐn)?shù)為29.9%時(shí),其共晶點(diǎn)溫度為-55℃。所以我們?cè)谶x擇鹽水溶液時(shí),鹽的含量一定要適中。過(guò)大和過(guò)小都是不利的。一般情況是使鹽水凝固點(diǎn)比系統(tǒng)中制冷劑蒸發(fā)溫度低4~8℃。
氯化鈉等鹽水溶液最大的缺點(diǎn)是對(duì)金屬有強(qiáng)烈的腐蝕作用。實(shí)踐證明,金屬被腐蝕與鹽水溶液中的含氧量有關(guān),含氧量越大,腐蝕性越強(qiáng)。鹽水中的氧主要來(lái)自空氣,為了減少含氧量最好采用封閉式鹽水系統(tǒng),減少與空氣接觸。此外,可向鹽水中加一定量的緩蝕劑,一般采用氫氧化鈉(NaOH)和重鉻酸鈉(Na2Cr2O7),溶液呈堿性反應(yīng)(pH值≈8.5),可用酚酞試劑測(cè)試。注意重鉻酸鈉有毒,能使皮膚破裂,有腐蝕作用,調(diào)配溶液時(shí)應(yīng)小心。
鹽水中加緩蝕劑最適宜的添加量為:
1m3氯化鈉鹽水溶液應(yīng)加入NaOH 0. 87kg, Na2Cr2O7 3. 2kg,1m3氯化鈣鹽水溶液應(yīng)加入NaOH 0. 32kg, Na2Cr2O7 1.6kg,重鉻酸鈉與氫氧化鈉的質(zhì)量之比應(yīng)為100:27,即每100kg重鉻酸鈉需加入27kg氫氧化鈉。
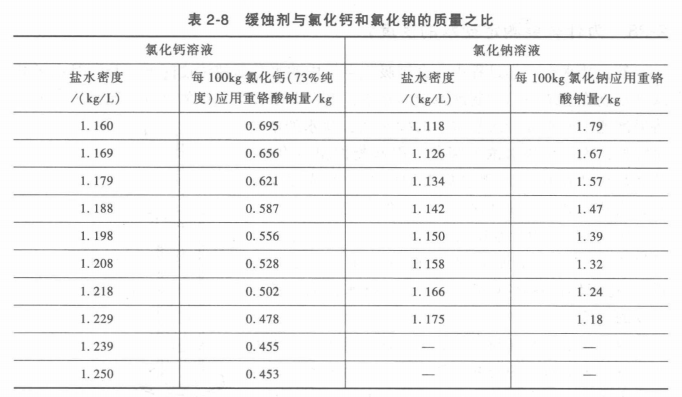
緩蝕劑與氯化鈣和氯化鈉的質(zhì)量之比見(jiàn)表2-8。